2020年上半年��,NMPA共批準(zhǔn)27個(gè)新藥上市���,包括17個(gè)進(jìn)口藥品和10個(gè)國(guó)產(chǎn)藥品�。從藥物類型來(lái)看���,包括13個(gè)化藥�、10個(gè)生物藥���、3個(gè)中藥和1個(gè)疫苗產(chǎn)品��。

注:此處所列新藥��,主要是指NMPA首次批準(zhǔn)在中國(guó)上市的藥品�,包括新分子實(shí)體(以及包含有新分子實(shí)體的復(fù)方)�、生物藥、中藥和疫苗�����。其中,新分子實(shí)體主要是化藥注冊(cè)分類下的1類(境內(nèi)外均未上市的創(chuàng)新藥)���、5.1類(境外上市的原研藥申請(qǐng)?jiān)趪?guó)內(nèi)上市)�����;生物藥主要是生物制品注冊(cè)分類下的1類(未在國(guó)內(nèi)外上市銷售的生物制品)�、2類(單克隆抗體)��。不包括生物類似物����、新適應(yīng)癥�����、新劑型�。
2020上半年在中國(guó)獲批上市的5.1類新藥中���,先聲藥業(yè)擁有阿巴西普的中國(guó)權(quán)益�,北?�?党菗碛心卫婺岬闹袊?guó)權(quán)益��,復(fù)星醫(yī)藥擁有阿伐曲泊帕的中國(guó)權(quán)益。另外�����,Asahi Kasei 公司的萘哌地爾和GSK的鹽酸安非他酮緩釋片屬于原研首次在中國(guó)上市��,國(guó)內(nèi)已有多家仿制藥獲批����。
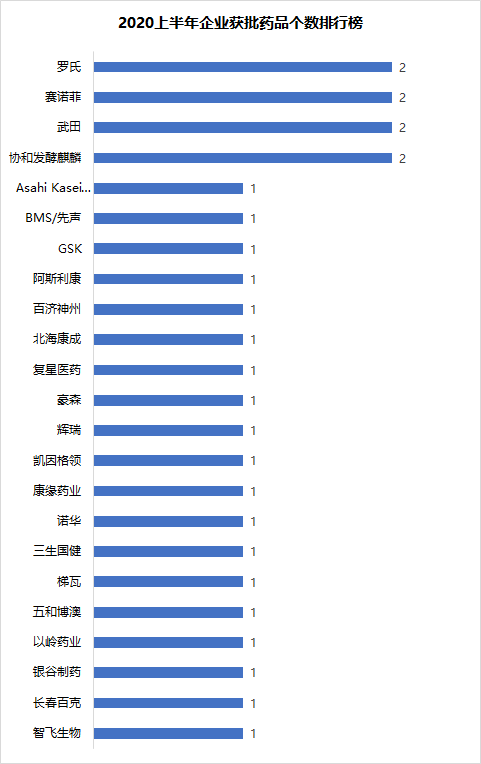
從企業(yè)來(lái)看,2020上半年���,羅氏����、武田��、賽諾菲和協(xié)和發(fā)酵麒麟均有2款新藥在中國(guó)獲批上市���。其中��,羅氏的恩美曲妥珠單抗為一個(gè)在國(guó)內(nèi)獲批上市的抗體偶聯(lián)藥物(ADC)���,阿替利珠單抗為第2個(gè)在中國(guó)獲批的PD-L1藥物��。武田的維布妥昔單抗則為第2個(gè)在中國(guó)獲批的ADC藥物��。
另外�,2020年獲批上市的17個(gè)進(jìn)口藥品中��,有6個(gè)屬于臨床急需境外用藥�。從審批天數(shù)來(lái)看��,除柏達(dá)魯單抗為遞交臨床申請(qǐng)后直接獲批上市外���,其余5個(gè)藥品平均審批時(shí)間為213天�����。其中,氘代丁苯那嗪片僅用時(shí)115天便在中國(guó)獲批上市��。
2020上半年獲批的臨床急需境外用藥
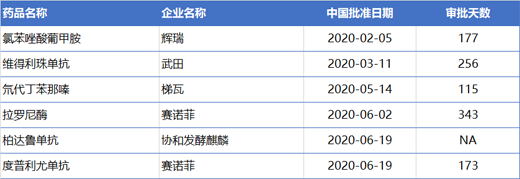
注:不包括新適應(yīng)癥申請(qǐng)
以下選取部分新藥做一簡(jiǎn)單介紹:
1.一個(gè)國(guó)內(nèi)獲批上市的抗體偶聯(lián)藥物
羅氏恩美曲妥珠單抗于2020年1月在中國(guó)獲批����,主要用于接受了紫杉烷類聯(lián)合曲妥珠單抗為基礎(chǔ)的新輔助治療后仍殘存侵襲性病灶的HER2陽(yáng)性早期乳腺癌患者的輔助治療,也填補(bǔ)了我國(guó)HER2陽(yáng)性乳腺癌患者在新輔助治療后未達(dá)到病理完全緩解(pCR)的治療空白。
該適應(yīng)癥在美國(guó)和歐盟獲批的時(shí)間分別為2019年5月和2019年12月�����,實(shí)現(xiàn)了中國(guó)和歐美國(guó)家的同步批準(zhǔn)�����。
2.近10年來(lái)一個(gè)糖尿病中藥新藥
五和博澳的桑枝總生物堿片主要用于配合飲食控制及運(yùn)動(dòng)治療2型糖尿病����。該藥III期臨床證明療效與阿卡波糖相似,是近10年來(lái)一個(gè)獲批的糖尿病中藥新藥�。
3.一個(gè)國(guó)產(chǎn)三代EGFR-TKI藥物
豪森的甲磺酸阿美替尼片主要用于既往經(jīng)表皮生長(zhǎng)因子受體(EGFR)酪氨酸激酶抑制劑(TKI)治療時(shí)或治療后出現(xiàn)疾病進(jìn)展,并且經(jīng)檢測(cè)確認(rèn)存在EGFR T790M突變陽(yáng)性的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌成人患者��。這是全球第3個(gè)三代EGFR-TKI創(chuàng)新藥���,也是一個(gè)國(guó)產(chǎn)三代EGFR-TKI藥物�。
4.一個(gè)氘代藥物
梯瓦的氘代丁苯那嗪片主要用于治療與亨廷頓病有關(guān)的舞蹈病及成人遲發(fā)性運(yùn)動(dòng)障礙�����。這是FDA批準(zhǔn)的一個(gè)氘代產(chǎn)品�����,也是針對(duì)與亨廷頓病有關(guān)的舞蹈病的歷史上第2個(gè)藥物。中國(guó)是繼美國(guó)之后第2個(gè)批準(zhǔn)該藥物的國(guó)家�����,這也是中國(guó)一個(gè)獲批的氘代藥物����。
5.一個(gè)國(guó)產(chǎn)BTK抑制劑
百濟(jì)神州的澤布替尼是一個(gè)獲得美國(guó)FDA批準(zhǔn)的本土研發(fā)抗癌新藥�,也是國(guó)內(nèi)一個(gè)上市的國(guó)產(chǎn)BTK抑制劑。目前����,百濟(jì)神州已經(jīng)在歐盟提交澤布替尼治療華氏巨球蛋白血癥患者的上市許可申請(qǐng)。
6.一個(gè)特應(yīng)性皮炎靶向生物制劑
賽諾菲Dupilumab注射液是全球一個(gè)獲批治療成人中重度特應(yīng)性皮炎的靶向生物制劑��。Dupixent是一款靶向IL-4R的單克隆抗體藥物����,于2017年3月首次獲得FDA批準(zhǔn)���,2019年全球銷售收入即達(dá)到20.74億歐元�����,賽諾菲計(jì)劃將其打造為年銷售額過(guò)100億歐元的重磅炸彈����。
聲明:本文版權(quán)歸原作者所有,轉(zhuǎn)載文章僅為傳播更多信息���,如作者信息標(biāo)記有誤�,或侵犯您的版權(quán)����,請(qǐng)聯(lián)系我們,我們將在及時(shí)修改或刪除內(nèi)容�,聯(lián)系郵箱:marketing@360worldcare.com


