甲狀旁腺功能減退激素替代療法獲FDA優(yōu)先審評����,有望明年初上市
10月31日��,Ascendis Pharma宣布���,F(xiàn)DA已受理TransCon PTH用于治療甲狀旁腺功能減退成人患者的新藥申請��,并授予其優(yōu)先審查資格�����,PDUFA日期為2023年4月30日��。如果獲批�,TransCon PTH將成為一個(gè)治療甲狀旁腺功能減退的激素替代療法。此前�����,TransCon PTH已被FDA和EMA授予治療甲狀旁腺功能減退的孤兒藥資格�����。
TransCon PTH是一種每日一次的長效甲狀旁腺激素(PTH)前藥�����,它旨在每天24小時(shí)將PTH恢復(fù)至生理水平����,以解決該疾病的短期癥狀和長期并發(fā)癥���。
甲狀旁腺功能減退癥(HP)是一種罕見的內(nèi)分泌疾病��,其特征是甲狀旁腺激素(PTH)水平不足�,導(dǎo)致血液中鈣含量降低和磷酸鹽水平升高��。大多數(shù)患者在甲狀腺手術(shù)期間受傷或意外切除甲狀旁腺后發(fā)生疾病��。鈣補(bǔ)充劑和活性維生素D的常規(guī)治療不能有效解決甲狀旁腺功能減退的短期癥狀、長期并發(fā)癥或?qū)ι钯|(zhì)量造成的影響��。目前尚無恢復(fù)生理激素水平的替代治療�。截至目前,甲狀旁腺功能減退癥是終末一種尚未實(shí)現(xiàn)真正的激素替代治療的內(nèi)分泌激素缺乏性疾病�����。
本次新藥申請基于全球III期PaTHway試驗(yàn)�、II期PaTH Forward 試驗(yàn)以及兩項(xiàng)正在進(jìn)行的開放標(biāo)簽擴(kuò)展研究的數(shù)據(jù)。PaTHway試驗(yàn)是一項(xiàng)雙盲�,安慰劑對照的III期試驗(yàn),旨在探討TransCon PTH對成人HP患者的療效���。該研究主要終點(diǎn)為治療26周后血鈣控制正常(8.3~10.6 mg/dL)且停用傳統(tǒng)治療(即停用活性維生素D且鈣劑≤600 mg/天)的患者比例�����;關(guān)鍵次要終點(diǎn)為HP患者體驗(yàn)量表(HPES)癥狀-軀體得分���、HPES癥狀-認(rèn)知得分、HPES影響-軀體功能量表得分�����、HPES影響-日常生活得分、SF-36軀體功能量表得分����。
TransCon PTH研究方案
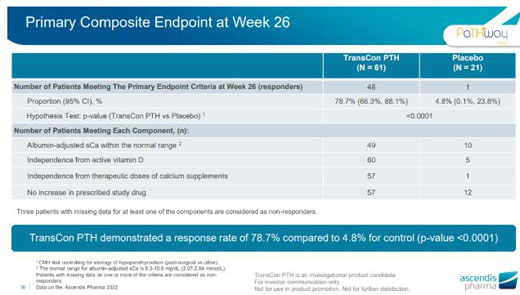
研究結(jié)果顯示,與對照組相比��,TransCon PTH組主要復(fù)合終點(diǎn)和所有關(guān)鍵性次要終點(diǎn)均出現(xiàn)統(tǒng)計(jì)學(xué)顯著改善��。78.7%接受TransCon PTH治療患者(48/61)達(dá)到了主要終點(diǎn)�����,而對照組這一數(shù)值為4.8%(p<0.0001)�����。通過甲狀旁腺功能減退患者體驗(yàn)量表(HPES)檢測的患者身體癥狀和認(rèn)知癥狀均實(shí)現(xiàn)統(tǒng)計(jì)學(xué)顯著減少���。安全性方面,TransCon PTH通常耐受良好���,無研究藥物相關(guān)停藥事件發(fā)生�。
TransCon PTH研究結(jié)果
Ascendis Pharma高級副總裁兼醫(yī)療官Dana Pizzuti說:“我們認(rèn)為治療甲狀旁腺功能減退癥的較佳方法是每天24小時(shí)將PTH恢復(fù)至生理水平��。美國患者目前還沒有這樣的治療方案,如果TransCon PTH獲得批準(zhǔn)����,其可能成為治療甲狀旁腺功能減退癥的根本療法?���!?/span>
維昇藥業(yè)(VISEN Pharmaceuticals)公司成立于2018年,是由維梧資本攜手丹麥生物制藥領(lǐng)軍企業(yè)Ascendis成立的創(chuàng)新型生物制藥獨(dú)角獸企業(yè)�����,專注于內(nèi)分泌領(lǐng)域創(chuàng)新藥的開發(fā)及商業(yè)化��,為生長激素缺乏癥���、甲狀旁腺功能減退癥����、軟骨發(fā)育不全等內(nèi)分泌罕見病提供全新���、專業(yè)和高效的治療方案���。維昇藥業(yè)獲得Ascendis Pharma授權(quán)�����,擁有其研發(fā)的包括TransCon PTH在內(nèi)三款內(nèi)分泌產(chǎn)品在大中華區(qū)特有開發(fā)�����、生產(chǎn)及商業(yè)化上市的權(quán)益���。目前,TransCon PTH正在國內(nèi)進(jìn)行III期臨床研究����。
聲明:本文版權(quán)歸原作者所有��,轉(zhuǎn)載文章僅為傳播更多信息�����,如作者信息標(biāo)記有誤�,或侵犯您的版權(quán),請聯(lián)系我們�����,我們將在及時(shí)修改或刪除內(nèi)容,聯(lián)系郵箱:marketing@360worldcare.com