和黃醫(yī)藥/創(chuàng)響生物新型BTK抑制劑獲批臨床,針對蕁麻疹!
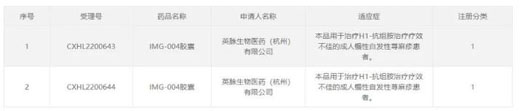
今日(11月28日)���,中國國家藥監(jiān)局藥品審評中心(CDE)官網(wǎng)公示����,一款研發(fā)代號(hào)為IMG-004的1類新藥獲得兩項(xiàng)臨床試驗(yàn)?zāi)驹S可����,擬開發(fā)用于治療特定的成人慢性自發(fā)性蕁麻疹患者。公開資料顯示����,IMG-004是一款新型的BTK抑制劑,起初由和黃醫(yī)藥發(fā)現(xiàn)�����,創(chuàng)響生物擁有該藥用于治療免疫性疾病的權(quán)利的選擇權(quán)���。
截圖來源:CDE官網(wǎng)
BTK屬于非受體酪氨酸激酶Tec家族����,參與某些免疫介導(dǎo)性疾病的先天性和適應(yīng)性免疫反應(yīng)。鑒于BTK在免疫反應(yīng)中的核心作用����,其抑制劑是針對一系列炎癥和自身免疫性疾病的潛在治療方法。
公開資料顯示�,IMG-004是一種非共價(jià)、可逆的小分子BTK抑制劑����,具有強(qiáng)效性、高選擇性和腦滲透性�。該藥起初由和黃醫(yī)藥發(fā)現(xiàn)。2021年1月�,創(chuàng)響生物與和黃醫(yī)藥達(dá)成戰(zhàn)略合作,以進(jìn)一步開發(fā)由和黃醫(yī)藥發(fā)現(xiàn)的四款用于治療多種免疫性疾病的候選藥物���,其中就包括本次獲批臨床的IMG-004����。
根據(jù)創(chuàng)響生物公開資料����,IMG-004是專門為通常需要長期治療的炎癥性和自身免疫性疾病患者而設(shè)計(jì)。在臨床前模型中,它已顯示出更好的活性�����、選擇性和藥代動(dòng)力學(xué)特征���。2022年8月,創(chuàng)響生物與和黃醫(yī)藥宣布����,IMG-004的全球1期臨床試驗(yàn)已在美國完成首例受試者給藥。這是一項(xiàng)隨機(jī)�、雙盲、安慰劑對照的單次和多次給藥劑量遞增研究�,旨在探索IMG-004在健康受試者中的安全性、耐受性����、藥代動(dòng)力學(xué)和藥效學(xué)等特性。
本次在中國����,IMG-004膠囊獲批的臨床研究適應(yīng)癥為H1-抗組胺治療療效不佳的成人慢性自發(fā)性蕁麻疹患者。慢性自發(fā)性蕁麻疹是一種難于預(yù)測的嚴(yán)重皮膚疾病�,其特征為出現(xiàn)瘙癢、疼痛性蕁麻疹、或/和腫脹���,持續(xù)至少6周����,且發(fā)生原因未知���。由于慢性自發(fā)性蕁麻疹的嚴(yán)重程度和不可預(yù)測性����,對患者的生活質(zhì)量造成嚴(yán)重影響��。盡管有治療方法���,在大部分患者中�����,這種疾病仍然沒有得到充分控制���。
希望IMG-004膠囊的后續(xù)臨床試驗(yàn)順利進(jìn)行,并取得好的結(jié)果�,早日為患者帶來新的治療選擇�。
聲明:本文版權(quán)歸原作者所有�,轉(zhuǎn)載文章僅為傳播更多信息,如作者信息標(biāo)記有誤�,或侵犯您的版權(quán),請聯(lián)系我們��,我們將在及時(shí)修改或刪除內(nèi)容�����,聯(lián)系郵箱:marketing@360worldcare.com