Nature:新發(fā)現(xiàn)��!腫瘤自身的代謝過程或許要比預(yù)想中更慢����!
科學(xué)家們從來都并不確切地知道在哺乳動物機體中癌變的腫瘤到底會消耗多少能量���,他們假設(shè)癌細(xì)胞會消耗大量能量,并攪動營養(yǎng)物質(zhì)�����,使得諸如心臟、肝臟和胰腺等健康器官處于一種不利的狀態(tài)���,因為代謝系統(tǒng)會擴散營養(yǎng)����。然而����,近日一篇發(fā)表在國際雜志Nature上題為“Slow TCA flux and ATP production in primary solid tumours but not metastases”的研究報告中,來自普林斯頓大學(xué)等機構(gòu)的科學(xué)家們通過研究發(fā)現(xiàn)���,事實或許恰恰相反����,即腫瘤將營養(yǎng)物質(zhì)轉(zhuǎn)化為可用的細(xì)胞能量的過程會明顯且可量化地減緩���。這種“昏睡”(lethargy)行為或許能幫助腫瘤為其更邪惡的行為來保存能量���,比如生長和轉(zhuǎn)移等。
在5種不同類型的癌癥中�����,研究者發(fā)現(xiàn),腫瘤會在低能量的環(huán)境中成功增殖����,部分是因為其忽略了健康器官為整個機體的利益而發(fā)揮的正常組織功能。這一研究發(fā)現(xiàn)對于新型抗癌療法的開發(fā)意義重大��,因為其能將注意力引向緩慢的能量代謝����。一些針對癌癥患者的治療建議會圍繞“餓死腫瘤”的策略,假設(shè)沒有營養(yǎng)物質(zhì)的話��,腫瘤就無法生長�,而從能量基質(zhì)的一般角度來看,這種策略充其量是值得懷疑的����。但研究人員確實發(fā)現(xiàn),腫瘤要比正常組織更會利用一種特殊的營養(yǎng)物質(zhì)�,即葡萄糖,因此這符合將標(biāo)準(zhǔn)癌癥療法與減少機體葡萄糖循環(huán)的飲食進(jìn)行結(jié)合的可能性���,比如生酮飲食等���。
研究者Caroline Bartman表示,我認(rèn)為人們假設(shè)癌癥需要很多能量的話���,因為其必須支付細(xì)胞分裂和增殖的“費用”�,但并沒有人真正測定過與機體健康器官相比癌癥會制造和使用多少能量��。為此��,研究人員開發(fā)了一種測定方法����,并發(fā)現(xiàn)了腫瘤和其它組織之間的巨大差異,如今研究人員擁有了一種范式����,即癌癥是非常節(jié)約的,其會停止將能量用于機體所有的健康任務(wù)��,而是將其用于增殖�����,這或許就告訴我們��,諸如餓死癌癥等類型的途徑以及單獨的治療策略或許并不是較好的。
腫瘤自身的代謝過程或許要比預(yù)想中更慢�����。
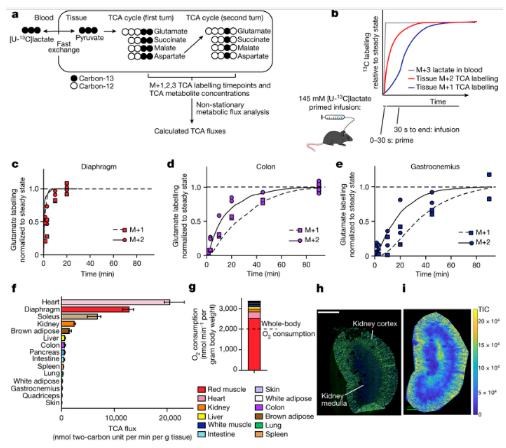
腫瘤會面臨更為殘酷的代謝環(huán)境�,因為其沒有在機體其它部位形成適當(dāng)?shù)难埽@或許就會迫使其以少勝多��;腫瘤在很多方面都是具有較高代謝特征的���,研究人員都能觀察到其較高的代謝過程�,而這也會支持其生長和分化的能力���。細(xì)胞的生長是昂貴的��,但并不像有思想或移動肌肉�,亦或者是擁有正常器官的哺乳動物生活的其它方面那樣昂貴���。為了量化這項研究�����,研究人員利用一種稱之為同位素追蹤(isotope tracing)的調(diào)查方法進(jìn)行研究��,該方法涉及利用重同位素來標(biāo)記營養(yǎng)物質(zhì)����,并監(jiān)測其在哺乳動物體內(nèi)代謝的速度。哺乳動物機體的組織和器官主要通過三羧酸循環(huán)(TCA)來為其所干的工作來賦予能量�,TCA能氧化脂肪和碳水化合物從而制造主要的能量—ATP���,95%的ATP(哺乳動物機體的可用能量)都是通過該循環(huán)所獲得的���,通過研究從血液中吸收營養(yǎng)物質(zhì)進(jìn)入到TCA循環(huán)的速度,研究人員就能定量癌癥組織和健康組織之間產(chǎn)生和使用能量的多少或水平�����。
比如�,在肺癌、胰腺癌和結(jié)腸癌中���,他們就發(fā)現(xiàn)���,原發(fā)性實體瘤中(即尚未開始擴散的腫瘤)的TCA通量和ATP的生產(chǎn)周期會較為緩慢。相比原發(fā)性腫瘤而言�����,轉(zhuǎn)移性癌癥會制造并利用更多能量,并且會與機體健康組織相當(dāng)?shù)乃缴献龅竭@一點�����。這或許就讓研究人員得出結(jié)論表明���,癌細(xì)胞會擺脫能量昂貴的組織特異性功能來為腫瘤的生長儲備能量��。這是研究人員在體內(nèi)對腫瘤的能量產(chǎn)生進(jìn)行量化研究��,并作為比較研究的一部分內(nèi)容���。
研究者Bartman說道,如今我們使用的一些方法此前已經(jīng)被其他研究人員使用過���,比如TCA循環(huán)的途徑大約在80年前被科學(xué)家們發(fā)現(xiàn)��,但技術(shù)的進(jìn)步和更好的光譜測定技術(shù)或許會提供令人吃驚的研究新發(fā)現(xiàn)�����。研究者認(rèn)為現(xiàn)在正是這一研究領(lǐng)域激動人心的時刻��,因為隨著過去50年的研究進(jìn)步���,現(xiàn)在或許是一個非常富有成效的hike�,研究人員可以重頭審視所有舊觀點并利用其來更好地理解諸如癌癥等疾病的發(fā)生機理�����。
綜上�,本文研究結(jié)果表明��,隨著實體瘤的進(jìn)展����,癌細(xì)胞會擺脫能量昂貴的組織特異性功能,而且在產(chǎn)生ATP能量有限的情況下仍能促進(jìn)癌細(xì)胞的失控生長���。
聲明:本文版權(quán)歸原作者所有�����,轉(zhuǎn)載文章僅為傳播更多信息�,如作者信息標(biāo)記有誤���,或侵犯您的版權(quán)�,請聯(lián)系我們,我們將在及時修改或刪除內(nèi)容�����,聯(lián)系郵箱:marketing@360worldcare.com