恒瑞JAK1抑制劑「艾瑪昔替尼」新適應(yīng)癥申報上市
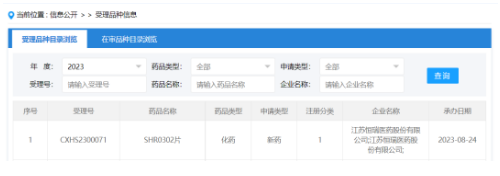
8月24日���,CDE官網(wǎng)顯示,恒瑞JAK1抑制劑艾瑪昔替尼片(SHR0302)新適應(yīng)癥的上市申請獲得受理�����。根據(jù)臨床試驗(yàn)進(jìn)展,推測本次申報上市的適應(yīng)癥為類風(fēng)濕性關(guān)節(jié)炎��。
SHR0302是恒瑞醫(yī)藥自主研發(fā)的高選擇性的JAK1抑制劑�����,國家1類新藥�����,是國內(nèi)自主研發(fā)的具有一類知識產(chǎn)權(quán)的口服小分子創(chuàng)新藥物��,可通過抑制JAK1信號傳導(dǎo)發(fā)揮抗炎和抑制免疫的生物學(xué)效應(yīng)�����。
SHR0302目前已開展了包括類風(fēng)濕性關(guān)節(jié)炎����、潰瘍性結(jié)腸炎���、特應(yīng)性皮炎����、斑禿、銀屑病關(guān)節(jié)炎等多領(lǐng)域的臨床研究���。2021年1月����,SHR0302片劑被國家藥監(jiān)局授予了突破性療法�,用于治療成人及12歲以上青少年的中重度特應(yīng)性皮炎,目前Ill期臨床結(jié)果已經(jīng)達(dá)到了共同主要終點(diǎn)及次要終點(diǎn)�����,恒瑞已于2023年6月遞交了該適應(yīng)癥的上市申請�。
2018年1月,恒瑞醫(yī)藥就SHR0302與美國Arcutis公司達(dá)成了合作協(xié)議����,按照協(xié)議的內(nèi)容,Arcutis獲得SHR0302項(xiàng)目在美國�、歐盟和日本的獨(dú)家臨床開發(fā)、注冊和市場銷售的權(quán)利�����,研發(fā)和銷售的SHR0302的許可劑型范圍為用于皮膚疾病治療的局部外用制劑����;恒瑞醫(yī)藥較多可獲得共2.23億美元的首付款和里程碑款����,外加銷售提成�����。
聲明:本文版權(quán)歸原作者所有����,轉(zhuǎn)載文章僅為傳播更多信息,如作者信息標(biāo)記有誤��,或侵犯您的版權(quán)���,請聯(lián)系我們�,我們將在及時修改或刪除內(nèi)容�����,聯(lián)系郵箱:marketing@360worldcare.com