CAR-T細胞療法在治療血液腫瘤方面取得了巨大成功,目前已有10種治療B細胞腫瘤與多發(fā)性骨髓瘤的CAR-T產(chǎn)品獲得NMPA與FDA批準上市����。與CAR-T細胞類似,T細胞受體工程化T細胞(TCR-T)也是一類經(jīng)工程化改造的T細胞��。不同于CAR-T細胞主要識別細胞表面抗原�,TCR-T細胞可以靶向細胞內(nèi)部抗原,在抗病毒與抗腫瘤免疫治療領(lǐng)域具有廣泛的應(yīng)用前景�,有望成為繼CAR-T細胞之后����,又一類重磅工程化T細胞藥物���。鑒于HLA基因的多樣性及TCR受體庫的復(fù)雜性�,篩選抗原特異性的TCR受體依然具有挑戰(zhàn)性����。
近年來,mRNA技術(shù)被成功地應(yīng)用于新冠病毒疫苗的研發(fā)��,今年諾貝爾醫(yī)學(xué)與生理學(xué)獎也授予了發(fā)明mRNA修飾技術(shù)的兩位科學(xué)家Katalin Karikó與Drew Weissman����。而被稱為mRNA2.0時代的環(huán)狀mRNA(circRNA)技術(shù)更是引發(fā)了廣泛關(guān)注,其具有生產(chǎn)成本低�����、蛋白水平表達高的優(yōu)勢�����,在免疫細胞治療領(lǐng)域具有重要的應(yīng)用潛力��。
近日�����,上海交通大學(xué)醫(yī)學(xué)院附屬第一人民醫(yī)院/上海市第一人民醫(yī)院張巖與宋獻民研究團隊聯(lián)合蘇州科銳邁德生物醫(yī)藥科技公司左熾健團隊����,在 Molecular Therapy 期刊發(fā)表了題為:Circular mRNA-based TCR-T offers a safe and effective therapeutic strategy for treatment of cytomegalovirus infection 的研究論文。
該研究報道了基于環(huán)狀mRNA技術(shù)的TCR-T細胞療法��,為臨床上造血干細胞移植后人巨細胞病毒(CMV)感染提供新的�����、更為安全有效的免疫治療策略�。
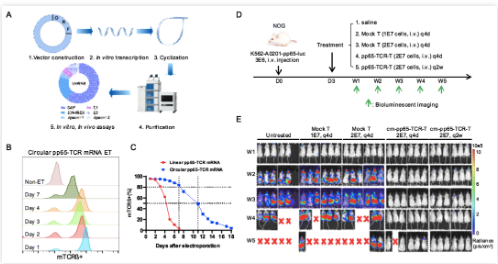
如何有效擴增抗原特異性T淋巴細胞并獲得抗原特異性TCR序列,是研發(fā)TCR-T細胞的關(guān)鍵�。蘇州科銳邁德生物醫(yī)藥科技公司之前的研究表明,環(huán)狀mRNA (circular mRNA, cmRNA)能夠顯著延長外源基因在細胞中的表達時長���。本項研究中���,研究團隊利用環(huán)狀mRNA技術(shù),在單核細胞分化的樹突狀細胞(moDCs)中表達CMV-pp65抗原,檢測是否能夠提供更為持久的抗原刺激信號���,促進抗原特異性T淋巴細胞的活化和增殖���。研究結(jié)果表明:與線性mRNA相比,轉(zhuǎn)染了編碼CMV-pp65 抗原的環(huán)狀RNA的moDCs細胞���,能更加持久地提供抗原信號���,更加高效地激活和擴增CMV-pp65特異性T細胞,表明基于環(huán)狀mRNA技術(shù)的抗原遞呈新策略����,能夠顯著提高TCR的篩選效率,在開發(fā)抗原特異性T細胞(尤其是含量較低的抗原特異性T細胞)方面具有巨大優(yōu)勢����。
此外,之前有文獻報道線狀mRNA編碼的TCR基因只能在原代T細胞中表達48-72小時��。研究團隊進而對環(huán)狀mRNA編碼的外源TCR基因在原代T淋巴細胞中的表達時長進行了測試����,發(fā)現(xiàn)環(huán)狀mRNA技術(shù)能夠顯著提升TCR基因在人原代T淋巴細胞中的表達時長�。在電轉(zhuǎn)后7天與11天�,依然分別有約80%與50%的T細胞表達外源TCR受體�����。研究團隊進一步對基于環(huán)狀mRNA技術(shù)的cm-pp65-TCR-T細胞在小鼠體內(nèi)的殺傷功能進行了測試���,體內(nèi)實驗結(jié)果表明���,兩周輸注一次cm-pp65-TCR-T細胞,即可有效清除表達CMV-pp65抗原的靶細胞���。
圖1. cm-pp65-TCR-T靶向清除表達CMV抗原的靶細胞
數(shù)據(jù)顯示�,我國人群CMV病毒感染率超過95%�����,多數(shù)呈現(xiàn)潛伏感染狀態(tài)����。然而,臨床上接受造血干細胞移植術(shù)的患者���,由于經(jīng)過術(shù)前清髓預(yù)處理�����,呈現(xiàn)暫時的T細胞免疫缺陷��,因而患者在移植后2-3個月CMV病毒易發(fā)生再激活���,發(fā)生CMV血癥甚至CMV肺炎�����。盡管來特莫韋等抗病毒藥物顯著降低了造血干細胞移植后患者CMV的再激活����,但對于部分患者而言CMV病毒再激活依然可能會危及患者生命�。
該研究將為這部分患者提供新的治療手段,因而具有重要的臨床研究意義���。多數(shù)造血干細胞移植患者在術(shù)后數(shù)月后��,體內(nèi)會重建針對CMV病毒的T細胞免疫�����?����;诃h(huán)狀mRNA技術(shù)的TCR-T細胞�����,由于TCR基因不會整合到基因組��,沒有潛在的致瘤風(fēng)險��,因而具有良好的安全性�����。此外��,如果采用造血干細胞移植供者來源的T淋巴細胞制備cm-pp65-TCR-T細胞���,回輸患者后不僅可以治療CMV病毒感染,而且能夠增強“移植物抗腫瘤效應(yīng)”(GVL)����,促進供者造血干細胞的植入�。目前�����,市一醫(yī)院血液科即將在本項研究基礎(chǔ)上���,開展研究者發(fā)起的臨床研究(IIT)�。
綜上所述��,該研究是將環(huán)狀mRNA技術(shù)應(yīng)用于TCR-T細胞的研發(fā)與制備��,不僅為造血干細胞移植后CMV感染的免疫治療提供新的策略���,也為其它抗病毒或抗腫瘤TCR-T療法提供新的思路�。
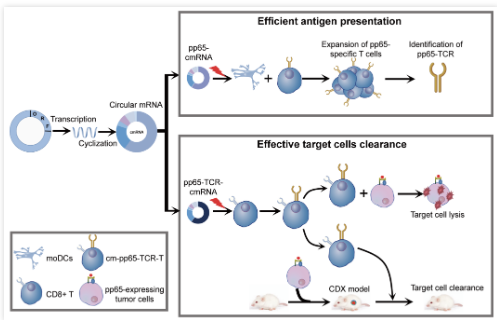
圖2. 基于環(huán)狀mRNA技術(shù)的TCR-T免疫療法示意圖
上海市第一人民醫(yī)院血液科博士研究生沈良華與蘇州科銳邁德生物醫(yī)藥科技公司楊嘉麗博士為文章的共同作者���。該研究使用的環(huán)狀mRNA由蘇州科銳邁德生物醫(yī)藥科技公司制備����,上海快序生物科技有限公司為本項研究提供抗原多肽質(zhì)譜分析����。
聲明:本文版權(quán)歸原作者所有����,轉(zhuǎn)載文章僅為傳播更多信息���,如作者信息標記有誤��,或侵犯您的版權(quán)���,請聯(lián)系我們,我們將在及時修改或刪除內(nèi)容�,聯(lián)系郵箱:marketing@360worldcare.com