近日,華中科技大學(xué)與浙江省臺(tái)州學(xué)院研究人員合作在權(quán)威期刊《Cell Death&Disease》上發(fā)表了題為“Blockade of DDR1/PYK2/ERK signaling suggesting SH2 superbinder as a novel autophagy inhibitor for pancreatic cancer”的研究論文���,本文中,研究人員采用免疫熒光和透射電鏡觀察自噬通量。使用無(wú)標(biāo)記的定量磷酸化蛋白質(zhì)組學(xué)來(lái)找出蛋白質(zhì)中酪氨酸磷酸化的嚴(yán)重改變���。并用荷瘤小鼠驗(yàn)證SH2 TrM-(Arg)9抑制腫瘤細(xì)胞的生長(zhǎng)。SH2 TrM-(Arg)9通過(guò)阻斷DDR1/PYK2/ERK信號(hào)級(jí)聯(lián)抑制膠原誘導(dǎo)的自噬���。SH2 TrM-(Arg)9提高了PANC-1/GEM細(xì)胞對(duì)吉西他濱(GEM)的敏感性�。SH2 TrM-(Arg)9對(duì)自噬的抑制可能與化療協(xié)同作用�����,并在胰腺癌異種移植中增強(qiáng)腫瘤抑制作用。研究結(jié)果表明�,SH2 TrM-(Arg)9可以通過(guò)抑制DDR1/PYK2/ERK信號(hào)傳導(dǎo)進(jìn)入PDAC細(xì)胞,阻斷自噬���,可能成為PDAC靶向治療的新治療策略��。
研究背景
胰腺癌(PC)是一種高度致命的消化系統(tǒng)惡性腫瘤�����,威脅著全世界數(shù)十萬(wàn)人的生命����,5年總生存率僅為12%�����。大約90%的胰腺惡性腫瘤是起源于胰腺導(dǎo)管上皮的胰腺導(dǎo)管腺癌(PDAC)��。由于胰腺的獨(dú)特位置和功能�����,許多PC患者在診斷時(shí)已處于中晚期;因此���,單純手術(shù)治療是無(wú)效的��?��;熗ǔJ侵委熗砥赑DAC的主要方法。吉西他濱(GEM)聯(lián)合紫杉醇或FOLFIRINOX(氟尿嘧啶���、伊立替康�、亞葉酸蛋白和奧沙利鉑)是目前的一線化療策略�。然而,由于化療耐藥和副作用�����,化療對(duì)晚期PDAC的療效有限�。其他治療方案,如靶向治療和免疫治療��,在一定程度上減緩了PDAC的發(fā)展���,但與化療相比沒(méi)有實(shí)質(zhì)性的優(yōu)勢(shì)����。此外,其中一些治療方案僅對(duì)一小部分具有特定基因型的患者有益���。因此���,有必要尋找療效更高、受益范圍更廣�、耐藥更少的新療法。
自噬是細(xì)胞在應(yīng)激或饑餓條件下回收生物分子并損傷細(xì)胞器的自我保護(hù)過(guò)程�����。自噬產(chǎn)生用于生物合成和能量生產(chǎn)的中間代謝物�����,并通過(guò)降解和再循環(huán)受損的DNA����、錯(cuò)誤折疊的蛋白質(zhì)和細(xì)胞內(nèi)病原體來(lái)促進(jìn)腫瘤生長(zhǎng)。PDAC腫瘤組織���、癌細(xì)胞和干細(xì)胞中均存在自噬通量異常激活�。PDAC腫瘤微環(huán)境中其他細(xì)胞(如胰腺星狀細(xì)胞)的自噬也為腫瘤的生長(zhǎng)發(fā)育提供能量��。許多研究表明��,自噬水平的增加可能是PDAC發(fā)展的重要原因���。因此�,抑制自噬被認(rèn)為是治療PDAC的重要策略���。迄今為止����,抑制自噬的小分子藥物和新型螯合劑在體外和體內(nèi)均顯示出良好的抗癌效果���。
研究進(jìn)展
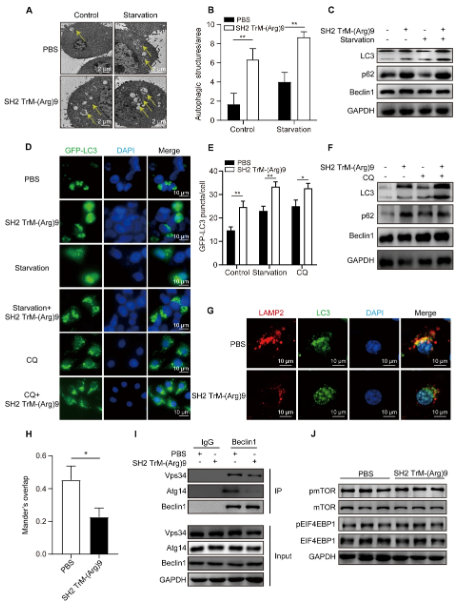
之前的研究表明SH2 TrM-(Arg)9具有抗腫瘤活性�����,并且具有廣泛的機(jī)制�����。然而�,SH2 TrM-(Arg)9與自噬之間的關(guān)系尚不清楚。利用透射電鏡觀察自噬體和自溶體�����,并探討SH2 TrM-(Arg)9是否會(huì)影響PDAC細(xì)胞的自噬�����。與先前的研究一致���,PDAC細(xì)胞在基礎(chǔ)條件下表現(xiàn)出較高的自噬���。如圖1(A、B)所示��,在SH2 TrM-(Arg)9處理的PANC-1細(xì)胞中�����,自噬體的數(shù)量明顯增加����,而在對(duì)照組中則沒(méi)有。接下來(lái)���,研究人員分析了LC3�����、p62和Beclin1的水平�。結(jié)果表明���,SH2 TrM-(Arg)9可誘導(dǎo)LC3的積累��。p62水平升高�,Beclin1無(wú)明顯變化�����。這一觀察結(jié)果也證實(shí)SH2 TrM-(Arg)9顯著增加了瞬時(shí)轉(zhuǎn)染GFP-LC3構(gòu)建體的GFP-LC3陽(yáng)性點(diǎn)的數(shù)量��。
圖1:SH2 TrM-(Arg)9抑制PANC-1細(xì)胞的自噬
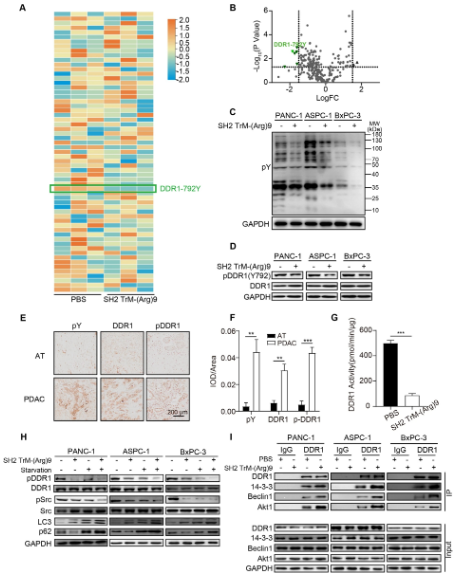
據(jù)報(bào)道�����,酪氨酸磷酸化的異常激活在人類標(biāo)本和PDAC細(xì)胞中起重要作用�����。為了揭示其生理活動(dòng)的分子機(jī)制,研究人員采用無(wú)標(biāo)記定量磷酸化蛋白質(zhì)組學(xué)的方法系統(tǒng)研究了SH2 TrM-(Arg)9引起的PANC-1細(xì)胞的全局磷酸化事件�����,希望找到在抗腫瘤過(guò)程中酪氨酸磷酸化的關(guān)鍵改變���。經(jīng)過(guò)三次獨(dú)立實(shí)驗(yàn)���,研究人員發(fā)現(xiàn)DDR1 (RTK家族成員)的Y792位點(diǎn)在三個(gè)來(lái)源的PANC-1細(xì)胞中呈現(xiàn)一致的變化趨勢(shì),這表明了該位點(diǎn)的重要性(數(shù)據(jù)集1)����。DDR1在自噬過(guò)程中在神經(jīng)系統(tǒng)疾病中發(fā)揮作用。在胰腺癌中���,阻斷膠原/ ddr1信號(hào)通路可抑制腫瘤生長(zhǎng);然而�����,其對(duì)自噬的影響尚不清楚����。從磷酸化蛋白質(zhì)組學(xué)結(jié)果來(lái)看��,研究人員發(fā)現(xiàn)SH2 TrM-(Arg)9處理組DDR1(Y792)的磷酸化酪氨酸水平顯著降低(圖2A, B)。為了進(jìn)一步證實(shí)磷酸化酪氨酸相關(guān)信號(hào)通路的重要性�,研究人員測(cè)量了酪氨酸(pY)和DDR1的磷酸化水平。數(shù)據(jù)顯示SH2 TrM-(Arg)9下調(diào)酪氨酸殘基的磷酸化水平(圖2C, D)�����。研究人員進(jìn)一步測(cè)量了PDAC和患者鄰近組織中總酪氨酸和DDR1(Y792)的磷酸化水平��。通過(guò)免疫染色���,研究人員發(fā)現(xiàn)腫瘤組織中pY和pDDR1(Y792)水平均升高(圖2E, F)。
圖2:阻斷DDR1/PYK2/ERK信號(hào)提示SH2超結(jié)合物是一種新的胰腺癌自噬抑制劑
研究結(jié)論
綜上所述�����,研究人員深入分析了SH2超粘結(jié)劑的作用機(jī)理�����。研究人員首次在PDAC細(xì)胞和動(dòng)物模型中發(fā)現(xiàn)SH2超結(jié)合物通過(guò)影響自噬而具有抗癌作用����。當(dāng)與GEM聯(lián)合使用時(shí),SH2超結(jié)合劑減少了化療耐藥性和副作用�����。基于SH2超結(jié)合物對(duì)PDAC細(xì)胞明顯的自噬抑制作用��,研究人員為再次將SH2超結(jié)合物作為抗癌藥物提供了證據(jù)支持�����,并且為PDAC的臨床治療提供了新的方向�����。
聲明:本文版權(quán)歸原作者所有����,轉(zhuǎn)載文章僅為傳播更多信息,如作者信息標(biāo)記有誤�����,或侵犯您的版權(quán)�,請(qǐng)聯(lián)系我們,我們將在及時(shí)修改或刪除內(nèi)容�,聯(lián)系郵箱:marketing@360worldcare.com