4月16日���,國家藥監(jiān)局網(wǎng)站顯示����,繼類風濕性關節(jié)炎和斑禿后�����,禮來的巴瑞替尼片在華獲批第3項適應癥�。
巴瑞替尼是Incyte開發(fā)的一款JAK抑制劑�,其片劑用法為每日口服1次。2009年12月�,禮來與Incyte達成協(xié)議,以7.55億美元的交易總額獲得該產(chǎn)品的共同開發(fā)和商業(yè)化權益��。
2017年2月��,巴瑞替尼片首次在歐盟獲批上市�����,商品名為Olumiant����,用于治療類風濕性關節(jié)炎。2019年7月�����,巴瑞替尼片在中國獲批。截至今日��,該產(chǎn)品在全球已獲批5項適應癥:1)類風濕性關節(jié)炎����;2)特應性皮炎;3)斑禿�;4)幼年特發(fā)性關節(jié)炎;5)新型冠狀病毒感染�。其中類風濕性關節(jié)炎和斑禿已在中國獲批。
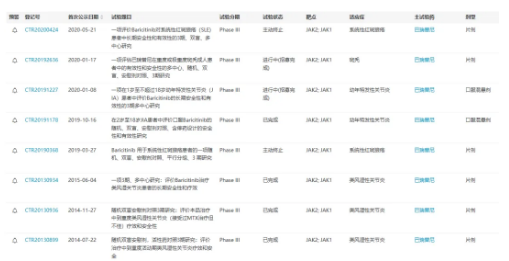
據(jù)公開信息�����,禮來就巴瑞替尼在中國開展了8項III期臨床試驗�,其中4項已標記為完成狀態(tài)��。
來源:醫(yī)藥魔方PharmaGO數(shù)據(jù)庫
一項中國幼年特發(fā)性關節(jié)炎患者參與的全球多中心III期研究(I4V-MC-JAHV)結果顯示��,與安慰劑組相比�,巴瑞替尼組患者(2-11歲服用混懸劑,12-17歲服用片劑)的疾病發(fā)作時間顯著減少(NE vs. 27.14周���,風險比為0.241��,p<0.0001)����。
據(jù)禮來財報,2023年巴瑞替尼片銷售額為9.23億美元��。
巴瑞替尼的化合物專利本將于2029年到期��,但其專利已在今年1月被南京斯帕克醫(yī)藥無效�����。南京優(yōu)科生物子公司南京力博維制藥開發(fā)的巴瑞替尼片仿制藥已于2023年10月獲批��,尚未進入市場�����。此外�,山東華鉑凱盛/安徽泰恩康制藥合作開發(fā)的巴瑞替尼片仿制藥也已申請上市。
聲明:本文版權歸原作者所有����,轉載文章僅為傳播更多信息,如作者信息標記有誤���,或侵犯您的版權����,請聯(lián)系我們,我們將在及時修改或刪除內容��,聯(lián)系郵箱:marketing@360worldcare.com