6月12日�,中國國家藥監(jiān)局藥品審評中心(CDE)官網(wǎng)公示,百時(shí)美施貴寶旗下新基(Celgene)公司申報(bào)的1類新藥golcadomide膠囊獲批臨床��,擬開發(fā)用于未經(jīng)治的高危大B細(xì)胞淋巴瘤����。根據(jù)百時(shí)美施貴寶公開資料,golcadomide是一款新型E3泛素連接酶Cereblon(CELMoD)分子�����,已經(jīng)在國際范圍內(nèi)處于3期臨床階段��。在針對B細(xì)胞淋巴瘤的1/2期臨床研究中�,該產(chǎn)品的客觀緩解率(ORR)達(dá)到91.1%。
公開資料顯示�,百時(shí)美施貴寶公司的蛋白穩(wěn)態(tài)(Protein Homeostasis)技術(shù)平臺使用多種不同的方法來達(dá)到降解靶標(biāo)蛋白的效果,其中包括被稱為CELMoD的分子膠類化合物��。它們通過與E3泛素連接酶Cereblon結(jié)合�����,改變其底物特異性,讓它能夠標(biāo)記與癌癥相關(guān)的蛋白����,促使它們降解���?�;谠撈脚_產(chǎn)生的多款CELMoD已經(jīng)進(jìn)入臨床開發(fā)階段�����,包括本次獲批臨床的golcadomide膠囊(CC-99282)�����,該產(chǎn)品針對非霍奇金淋巴瘤(NHL)疾病特點(diǎn)做了優(yōu)化�,使其主要分布在淋巴器官�。
▲Golcadomide膠囊產(chǎn)品特點(diǎn)(圖片來源:參考資料[2])
2023年12月,百時(shí)美施貴寶宣布在美國血液學(xué)會(ASH)年會上公布了golcadomide的早期研究結(jié)果����。其中CC-220-DLBCL-001研究是一項(xiàng)1b期研究的劑量擴(kuò)展階段研究,探索了golcadomide與R-CHOP組合在既往未治療的侵襲性B細(xì)胞淋巴瘤患者中的活性和安全性�?;颊咭?:1的比例隨機(jī)分配到兩種推薦的2期劑量水平加R-CHOP-21�����,固定療程6個(gè)周期�����。
根據(jù)ASH官網(wǎng)公示�,研究結(jié)果顯示,中位隨訪時(shí)間為4.1個(gè)月時(shí)�,在所有治療結(jié)束有反應(yīng)的患者中,21/25(84%)達(dá)到完全代謝緩解率(CMR)����;共有14/14(100%)接受golcadomide 0.4mg劑量治療的患者在治療結(jié)束時(shí)達(dá)到了CMR。在可評估療效的患者(n=56)中�,ORR為91.1%。此外��,在兩個(gè)劑量組中��,穩(wěn)態(tài)水平的golcadomide將Ikaros降低了80%以上�����,達(dá)到預(yù)期的優(yōu)化腫瘤細(xì)胞殺傷和刺激T細(xì)胞和NK細(xì)胞的水平。
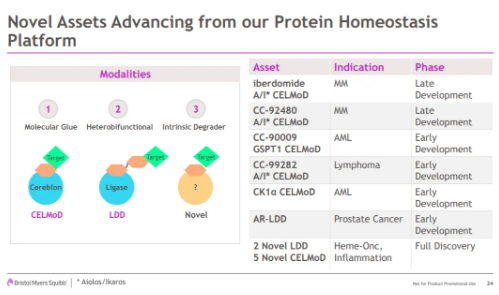
▲百時(shí)美施貴寶公司基于蛋白穩(wěn)態(tài)技術(shù)平臺開發(fā)的新分子(圖片來源:參考資料[2])
根據(jù)百時(shí)美施貴寶公開資料�����,golcadomide代表了該公司差異化的靶向蛋白降解劑研究平臺的核心產(chǎn)品之一���。除了該藥,百時(shí)美施貴寶還有多款靶向蛋白降解劑已經(jīng)在中國進(jìn)入臨床研究階段�����,比如CC-92480(mezigdomide)�����、iberdomide膠囊均已經(jīng)在中國啟動(dòng)3期臨床�,它們針對的適應(yīng)癥為多發(fā)性骨髓瘤。此外���,在國際范圍內(nèi)���,百時(shí)美施貴寶公司靶向GSPT1的分子膠類蛋白降解劑CC-90009、雄激素受體(AR)降解劑AR-LDD、針對血液系統(tǒng)惡性腫瘤的CK1α Degrader也正在1期臨床階段中進(jìn)行探索���。
聲明:本文版權(quán)歸原作者所有�����,轉(zhuǎn)載文章僅為傳播更多信息��,如作者信息標(biāo)記有誤��,或侵犯您的版權(quán)��,請聯(lián)系我們�,我們將在及時(shí)修改或刪除內(nèi)容��,聯(lián)系郵箱:marketing@360worldcare.com