迪哲醫(yī)藥JAK1抑制劑「戈利昔替尼」在中國獲批
今日(6月19日)�,迪哲醫(yī)藥宣布��,該公司自主研發(fā)的1類新藥高選擇性JAK1抑制劑戈利昔替尼膠囊(商品名:高瑞哲)正式獲得中國國家藥品監(jiān)督管理局(NMPA)批準(zhǔn)上市,單藥適用于既往至少接受過一線系統(tǒng)性治療的復(fù)發(fā)或難治的外周T細(xì)胞淋巴瘤(r/r PTCL)成人患者��。迪哲醫(yī)藥新聞稿指出���,這也是一個獲批用于治療PTCL的JAK1抑制劑。
PTCL是一種起源于胸腺后成熟T/NK細(xì)胞的惡性腫瘤����,在所有非霍奇金淋巴瘤中生存率較低。一線治療后緩解的患者存在極高復(fù)發(fā)風(fēng)險����,r/r PTCL患者的生存預(yù)后極差。然后��,針對這一群體的既往單藥治療效果極為有限�����,并且該領(lǐng)域在中國近十年沒有創(chuàng)新藥上市��,患者亟需新的治療選擇�。
迪哲醫(yī)藥專注于惡性腫瘤、免疫性疾病領(lǐng)域創(chuàng)新療法的研究�����、開發(fā)和商業(yè)化,其在研究中發(fā)現(xiàn)并驗(yàn)證了JAK-STAT通路是治療PTCL的高潛力干預(yù)靶點(diǎn)����,并基于此開發(fā)了高選擇性JAK1抑制劑戈利昔替尼。根據(jù)迪哲醫(yī)藥新聞稿��,戈利昔替尼獨(dú)特的“兩氫鍵一鹽橋”創(chuàng)新分子結(jié)構(gòu)設(shè)計(jì)���,使其對JAK1的選擇性高于對JAK家族其它成員200-400倍���,從而可以在大幅提升PTCL 治療效果的同時確保更好的臨床治療安全性。
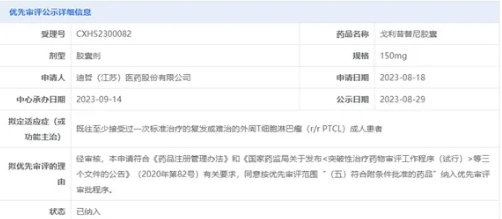
2023年9月��,中國國家藥監(jiān)局藥品審評中心(CDE)將戈利昔替尼的上市申請納入了優(yōu)先審評���,用于r/r PTCL的治療���,這也是該藥本次獲批的適應(yīng)癥。
截圖來源:CDE官網(wǎng)
戈利昔替尼膠囊此次獲批是基于全球關(guān)鍵性注冊臨床研究“JACKPOT8 B部分”(JACKPOT8 Part B����、JACKPOT8B)���,該研究旨在評估戈利昔替尼膠囊治療r/r PTCL的療效和安全性,研究的主要終點(diǎn)為獨(dú)立影像評估委員會(IRC)評估的客觀緩解率(ORR)����。該研究結(jié)果已在2023年第65屆美國血液學(xué)會(ASH)年會上以口頭報告形式公布���,并同步發(fā)表于《柳葉刀·腫瘤學(xué)》(Lancet Oncology)��。
研究數(shù)據(jù)顯示�,戈利昔替尼膠囊單藥治療r/r PTCL在緩解率��、不同亞型PTCL患者以及生存期方面均表現(xiàn)出了優(yōu)異的效果:
經(jīng)IRC確認(rèn)的ORR達(dá)44.3%��,完全緩解(CR)率達(dá)23.9%�,均是既往靶向治療方案近2倍;
在不同亞型PTCL中均觀察到腫瘤緩解����,滿足了既往藥物無法覆蓋的PTCL亞型的治療需求;
中位緩解持續(xù)時間(DoR)長達(dá)20.7個月(現(xiàn)有其它療法的DoR小于12個月)���。
JACKPOT8研究主要研究者��、北京大學(xué)腫瘤醫(yī)院朱軍教授表示:戈利昔替尼具有新機(jī)制����、新結(jié)構(gòu),是全球首款針對PTCL的口服JAK1高選擇性抑制劑�,具有良好的藥代動力學(xué)特性,是唯一在淋巴瘤領(lǐng)域有突破的JAK抑制劑�。戈利昔替尼具有使PTCL全亞型獲益的潛質(zhì),單藥治療r/r PTCL ORR達(dá)到44.3%����,DoR達(dá)到20.7個月,它的獲批上市有望沖破PTCL治療瓶頸�����,為PTCL診療帶來新格局�����。
迪哲醫(yī)藥創(chuàng)始人��、董事長兼首席執(zhí)行官張小林博士表示:戈利昔替尼作為全球首個且唯一治療PTCL的高選擇性JAK1抑制劑���,也是迪哲醫(yī)藥在一年內(nèi)成功上市的第2款源頭創(chuàng)新藥��。憑借全新作用機(jī)制���,戈利昔替尼能有效治療各亞型PTCL��,填補(bǔ)了既往藥物在多個亞型治療上的空白��。
根據(jù)迪哲醫(yī)藥新聞稿����,國際多中心關(guān)鍵性注冊臨床研究“JACKPOT8 B部分”(JACKPOT8B)正在中國��、美國�、韓國和澳大利亞等國家開展��。2022年2月�����,美國FDA已授予戈利昔替尼快速通道資格�����,用于治療r/r PTCL����。迪哲醫(yī)藥在新聞稿中表示�,該公司也將加速戈利昔替尼的全球研發(fā)進(jìn)程�����,力爭早日為全世界更多患者提供更優(yōu)治療選擇����。
作為迪哲醫(yī)藥的CDMO合作伙伴,藥明康德子公司合全藥業(yè)賦能了戈利昔替尼的成功開發(fā)�。據(jù)悉,合全藥業(yè)提供了涵蓋原料藥與制劑的研發(fā)�、生產(chǎn)、分析等一體化支持���,并于2024年1月順利通過了NMPA對戈利昔替尼的上市批準(zhǔn)前檢查(PAI, Pre-Approval Inspection)��,為該款新藥早日在中國獲批上市提供了強(qiáng)有力的保障�。未來����,合全藥業(yè)還將繼續(xù)為戈利昔替尼提供商業(yè)化供應(yīng)服務(wù)。
聲明:本文版權(quán)歸原作者所有�,轉(zhuǎn)載文章僅為傳播更多信息�����,如作者信息標(biāo)記有誤���,或侵犯您的版權(quán),請聯(lián)系我們����,我們將在及時修改或刪除內(nèi)容,聯(lián)系郵箱:marketing@360worldcare.com