7月23日,蘇州大學趙軍研究團隊在期刊《Cell Death&Disease》上發(fā)表了研究論文,題為“BUB1b impairs chemotherapy sensitivity via resistance to ferroptosis in lung adenocarcinoma”�,本研究中,研究人員發(fā)現(xiàn)BUB1b的轉錄和蛋白水平在腫瘤組織中顯著上調,并與肺腺癌患者的不良預后有關。此外,在體外和體內進行的功能獲得和功能缺失實驗證實����,BUB1b增強了LUAD細胞的活力���。機制上�����,BUB1b與OTUD3和NRF2形成復合體���,并穩(wěn)定下游NRF2信號通路,從而促進鐵死亡和化療的不敏感性�。在過表達BUB1b的BALB/c裸鼠皮下移植瘤中,ML385靶向聯(lián)合化療具有協(xié)同作用�,抑制腫瘤生長,明顯提高生存期�����。綜上所述�����,本研究揭示了BUB1b促進肺腺癌進展的潛在機制�,并提出了增強化療療效的新策略。
背景知識
肺癌仍然是全球癌癥相關死亡的主要原因����,其中肺腺癌(LUAD)是常見的組織學類型,占所有肺癌病例的40%以上���。除了根治性手術�,如肺葉或肺段切除聯(lián)合或不聯(lián)合輔助化療或放療����,更精準的治療,如EGFR靶向治療和免疫治療��,改善了肺腺癌患者的生存�����。EGFR激酶抑制劑已發(fā)展為第三代奧希替尼���,并在EGFR突變的晚期LUAD患者中取得了良好的療效�����。然而����,預后仍然很差,5年總生存率(OS)約為16%����,根據(jù)新的TNM分期系統(tǒng),5年復發(fā)率從I期的約20%到III期的50%不等�。因此,更好地了解促進LUAD進展的潛在機制對進一步改善預后至關重要�。
BUB1b (BUB1有絲分裂檢查點絲氨酸/蘇氨酸激酶B)屬于紡錘體家族,在有絲分裂過程中負責染色體和紡錘體的附著��。是一種多功能蛋白���,與CDC20��、BUB3和MAD2形成復合物���,從而破壞后期促進復合體或環(huán)體的功能���。鑒于BUB1b在調控染色體分離中的關鍵作用���,BUB1b的異常表達可能導致染色體不穩(wěn)定和癌癥發(fā)病率增加����。BUB1b對不同癌癥的影響也具有異質性��。在結腸腺癌中����,BUB1b的沉默促進了腫瘤的發(fā)生和發(fā)展,而在肝細胞癌�、胰腺導管腺癌和其他癌癥中則觀察到相反的現(xiàn)象。雖然之前的研究報道了BUB1b在肺癌中的致癌作用�,但BUB1b介導肺癌進展的潛在機制仍不清楚。
BUB1b通過靶向NRF2賦予LUAD的鐵死亡抗性
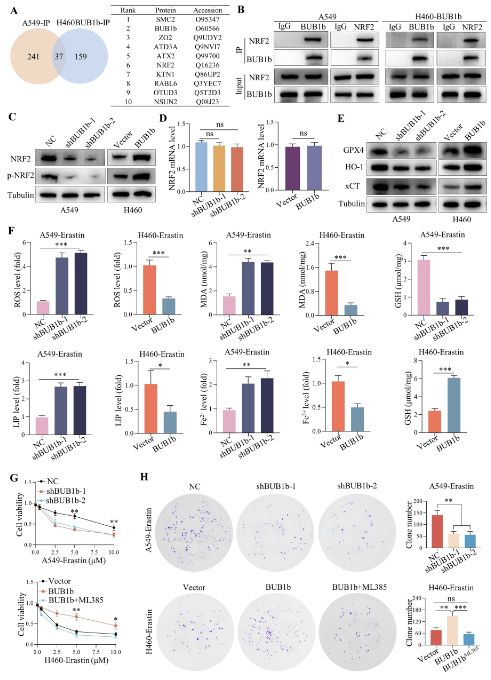
為了探索BUB1b促進肺腺癌進展的機制���,研究人員使用BUB1b抗體在A549和BUB1b過表達的H460細胞(H460-BUB1b)中進行了免疫沉淀(IP)實驗�����,并采用LC/MS檢測免疫共沉淀復合物����。在A549和H460-BUB1b-IP中分別檢測到278和196種蛋白,其中37種蛋白在兩種細胞中存在重疊����。在A549和H460-BUB1b細胞中排名前十的候選基因中,研究人員確定了轉錄因子NRF2�,它是鐵死亡通路的關鍵介質。因此�,研究人員推測BUB1b通過與NRF2的相互作用增強了LUAD的進展,并阻礙了鐵死亡通路的激活�。免疫共沉淀(Co-IP)檢測BUB1b和NRF2在A549和H460-BUB1b細胞中的表達,發(fā)現(xiàn)BUB1b和NRF2之間存在相互作用�。此外,在A549細胞中敲低BUB1b可降低NRF2和p-NRF2的蛋白水平���,在H460細胞中過表達BUB1b可升高NRF2和p-NRF2的蛋白水平�����,而在A549和H460細胞中NRF2的轉錄水平不依賴于BUB1b���,提示BUB1b可在轉錄后水平介導NRF2的穩(wěn)定性。
圖1:BUB1b通過靶向NRF2賦予LUAD的鐵死亡抗性
研究人員同時檢測NRF2的下游成分,免疫印跡結果顯示�,在BUB1b沉默后,GPX4�����、xCT和HO-1均下調�����,在BUB1b沉默的A549或BUB1b過表達的H460細胞中均升高����。此外��,活性氧(ROS)���、丙二醛(MDA)���、不穩(wěn)定鐵池(LIP)和Fe2+水平在A549-shBUB1b細胞中升高,而在H460-BUB1b細胞中降低�����。相反,抗氧化成分谷胱甘肽(GSH)在A549-shBUB1b細胞中顯著降低�,而在H460-BUB1b細胞中顯著升高。此外���,在鐵死亡誘導劑埃拉斯汀存在的情況下����,ROS����、MDA、GSH�����、LIP和Fe2+的變化趨勢相似�����。敲低BUB1b的A549細胞對埃拉斯汀的敏感性增加�,而過表達BUB1b的H460細胞對埃拉斯汀的耐藥性增加,而給予NRF2抑制劑ML385可進一步消除這種耐藥性����。在克隆形成實驗中��,敲低BUB1b也提高了埃拉斯汀的效率���,而ML385逆轉了由強制表達BUB1b引起的不敏感。研究人員還在A549-shBUB1b-1和A549-shBUB1b-2中過表達NRF2���。因此��,NRF2過表達增強了A549-shBUB1b-1和A549-shBUB1b-2的活力��。另外�����,在敲低BUB1b的A549細胞中,增強NRF2的表達可以恢復生長抑制和恢復對埃拉斯汀的耐藥性�����。埃拉斯汀處理后����,H460-BUB1b中NRF2的水平也升高,而A549-shBUB1b-1和A549-shBUB1b-2中NRF2的水平降低�����。因此,BUB1b可以通過在轉錄后水平穩(wěn)定NRF2來賦予肺腺癌的鐵死亡抗性�����。
ML385可使BUB1b高表達的肺腺癌細胞對化療增敏
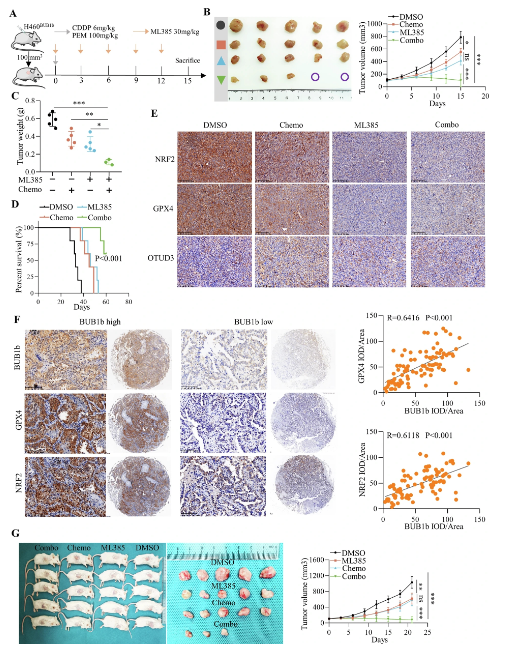
上述結果表明�����,BUB1b通過招募OTUD3穩(wěn)定NRF2����,產生鐵死亡抵抗,從而增強對化療的不敏感性�。于是,研究人員進一步探索了ML385和化療在體內環(huán)境下的協(xié)同作用��。研究人員構建了BALB/c裸鼠皮下移植瘤模型����,當腫瘤達到100 mm3時給予CDDP/PEM 1次,ML385每3天給予1次��。與單純化療或單純ML385相比���,ML385和化療的雙重阻斷顯著延緩了腫瘤的生長���,有2例在2周后腫瘤生長完全消失���。同樣,ML385和化療雙重阻斷給體內BUB1b高表達的LUAD帶來了更大的生存獲益���。免疫組織化學染色結果顯示��,化療+ ML385組鐵死亡陰性調控因子NRF2和GPX4明顯減少�����。此外���,通過免疫組織化學染色���,研究人員進一步研究了BUB1b, NRF2和GPX4在包含92例肺腺癌組織和配對癌旁組織的TMA中的關系���。結果顯示BUB1b與NRF2、GPX4呈正相關��。另外,研究人員還在5個肺腺癌患者來源的異種移植模型中研究了ML385和CDDP/PEM的協(xié)同作用��。同樣����,與單藥治療相比,ML385聯(lián)合CDDP/PEM顯著抑制了腫瘤生長����。
圖2:ML385使BUB1b高表達的LUAD細胞對化療敏感
研究小結
綜上所述,本研究揭示了BUB1b對肺腺癌鐵死亡和化療耐藥的影響��,并為BUB1b高表達的肺腺癌患者的化療增敏提供了新的策略����。BUB1b-NRF2-OTUD3復合物增強NRF2信號通路,抑制鐵死亡�,誘導化療耐藥。
聲明:本文版權歸原作者所有�����,轉載文章僅為傳播更多信息��,如作者信息標記有誤�����,或侵犯您的版權,請聯(lián)系我們��,我們將在及時修改或刪除內容�����,聯(lián)系郵箱:marketing@360worldcare.com